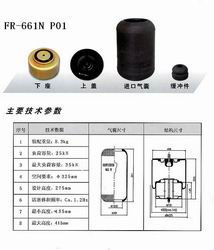
隨著工業自動化與減震技術需求的不斷提升,空氣彈簧作為一種高性能的彈性元件,在設備減震、精密儀器支撐、交通運輸等領域發揮著日益重要的作用。本文主要圍繞dokmd31100000型號空氣彈簧的采購要點,并結合其在熱壓平板機中的應用,提供一份綜合性的技術采購與應用指南。
一、dokmd31100000空氣彈簧采購核心考量
采購dokmd31100000空氣彈簧時,需重點關注以下技術參數與供應商資質:
- 技術規格確認:明確所需空氣彈簧的具體尺寸、工作壓力范圍、承載能力、行程以及連接方式(如法蘭或螺紋接口),確保與現有設備或設計圖紙完全匹配。
- 材質與工藝:優質的橡膠氣囊與高強度簾線層是保證耐久性和密封性的關鍵。應優先選擇采用耐油、耐老化、耐高低溫特種橡膠及精密成型工藝的產品。
- 性能與認證:核查產品是否通過相關行業標準(如ISO、GB等)測試,關注其疲勞壽命、動態響應特性及在極端工況下的穩定性報告。
- 供應商選擇:評估供應商的技術支持能力、售后服務網絡、歷史項目案例及交貨周期。選擇有信譽的品牌或授權代理商,以確保產品質量和穩定的供貨渠道。
- 成本與價值:在預算范圍內,綜合權衡產品價格、使用壽命、維護成本及對生產效率的潛在影響,追求最優的全生命周期成本。
二、空氣彈簧在熱壓平板機中的關鍵作用
熱壓平板機在復合材料成型、板材加工等行業應用廣泛,其工作過程要求平板具有極高的平行度、穩定的壓合力和有效的振動隔離。dokmd31100000等型號的空氣彈簧在此扮演了核心角色:
- 精密調平與壓力控制:空氣彈簧通過內部氣壓的精確調節,可以實時、微幅地調整熱壓板上方的支撐力,補償機械誤差或熱變形,確保整個壓板工作面壓力均勻,這對于保證產品成型質量至關重要。
- 高效減震與隔振:熱壓機在合模、加壓過程中可能產生沖擊和振動。空氣彈簧優秀的阻尼特性能夠有效吸收并隔離這些振動,保護精密模具和設備結構,同時減少噪音,改善工作環境。
- 延長設備壽命:通過替代傳統的剛性支撐或機械彈簧,空氣彈簧的柔性緩沖減少了設備關鍵部件所受的應力峰值和疲勞損傷,從而顯著延長熱壓平板機整體的使用壽命,降低維護頻率和成本。
三、采購與應用一體化建議
為保障熱壓平板機系統的可靠運行,建議采取以下一體化策略:
- 協同設計與選型:在設備設計或改造初期,即與空氣彈簧供應商的技術團隊溝通,根據熱壓機的具體噸位、工作頻率、溫度環境及精度要求,共同確定最適配的dokmd31100000空氣彈簧規格和安裝布局方案。
- 系統集成測試:采購后,在裝機前可要求供應商提供模擬工況下的性能測試數據。裝機完成后,應進行嚴格的空載與負載測試,驗證調平精度、壓力均勻性和減震效果是否達到預期目標。
- 建立維護規程:將空氣彈簧納入設備的定期點檢與預防性維護計劃。定期檢查氣囊有無龜裂、漏氣,清潔周邊環境,并監測氣壓系統的穩定性。儲備關鍵備件以應對突發故障。
###
dokmd31100000空氣彈簧的采購絕非簡單的物料購買,而是一項影響設備核心性能的技術決策。尤其是在熱壓平板機這類高精度、高要求的設備上,選擇合適的空氣彈簧并科學應用,是提升產品質量、保障生產效率和實現設備長期穩定運行的關鍵一環。采購方應秉持技術先行、質量為本的原則,與可靠的合作伙伴攜手,最大化發揮這一先進彈性元件的技術價值。